
Wie kann man Wärme transportieren?
Da Wärme eine Energie-Form ist, kann sie nur durch irgendwelche Massen bzw. Stoffe transportiert werden.
Die Schubkarre wird also nicht wirklich funktionieren.
Wärme könnte man dadurch transportieren, indem man z.B. einen Stahlblock aufheizt und dann dort hinschiebt, wo man die Wärme haben will, aber eben nur theoretisch. Mit Kälte gab's das in der Tat schon. Anfang des 19-ten Jahrhunderts wurde noch Eis in den Alpen geerntet und an Menschen verkauft, die damit Nahrungsmittel kühl lagern wollten. Erst mit der Erfindung einer Kältemaschine von Carl von Linde, die er 1876 präsentierte, war es möglich, Kälte dort zu erzeugen, wo sie gebraucht wurde.
Wärmetransport mit flüssigen oder gasförmigen Medien
--------------------------------------------------------------------------
Der Transport von Wärme mit Flüssigkeiten ist schon wesentlich einfacher. So funktionieren Zentralheizungen in vielen Häusern. Neben dem Heizungswasser ist auch immer wieder warme Luft im Einsatz. Das Grundprinzip ist aber immer dasselbe: Wärme wird von einem wärmeren Medium an ein kälteres abgegeben (zweiter Hauptsatz der Thermodynamik).
Die Physik hat aber einige kleine Überraschungen parat, die für sich gesehen nur wenig spektakulär erscheinen. So kennt man das Phänomen, dass Wasser zwar auf Meereshöhe bei 100° Celsius zu sieden beginnt, jedoch auf der Zugspitze in knapp 3000 m Höhe kocht es bereits bei ca. 90° Celsius und auf dem höchsten Berg der Erde, dem Mount Everest, in 8848 m Höhe, kocht Wasser bereits bei ca. 70° Celsius. Aber woher kommt das? Ganz einfach, daran ist der Luftdruck schuld. Je niedriger der Luftdruck ist, desto niedriger ist auch die Siedetemperatur. Der Unterschied beträgt nur rund 700 mbar! Genutzt wird dieser Effekt beispielsweise bei Schnellkochtöpfen. Dort wird mit dem Verdampfen von Wasser in einem abgedichteten Topf der Druck erhöht und dadurch eine höhere Siedetemperatur erreicht, die ihrerseits wiederum das Kochgut bei Temperaturen über 100° Celsius schneller garen lässt.
Die Frage ist also: Wie können wir diese Erkenntnis sinnvoll und effektiv nutzen für unseren Wärmetransport?
Dazu schauen wir uns einmal an, welche Wärmemengen bewegt werden müssen, um 1 kg Wasser von 10° Celsius auf Siedetemperatur zu bringen, bzw. wie viel Energie notwendig ist, um dieses Wasser zu verdampfen.
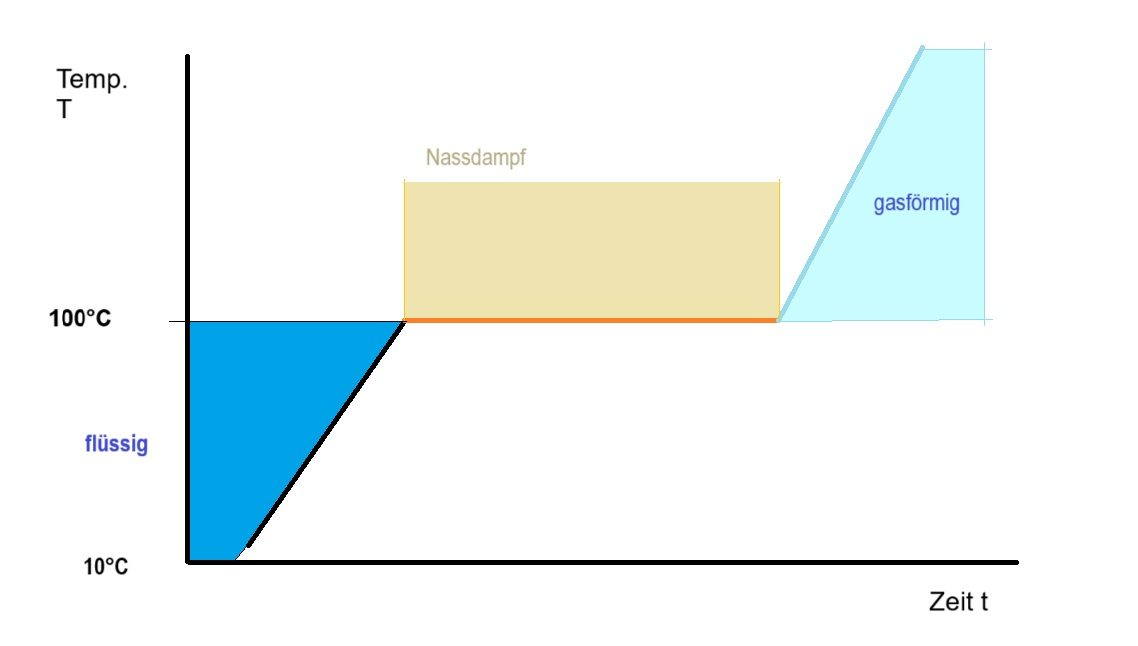
Das Erwärmungs-Diagramm von H2O
Wasser ist bei Temperaturen von größer 0°C bis zum Siedepunkt flüssig und ein Liter, bzw. 1 kg, benötigt ca. 4,18 kJ Wärmeenergie damit es sich um ein Grad erwärmt.
Also sind 90 * 4,18 kJ = 376,2 kJ erforderlich um 1 kg Wasser von 10° auf 100° Celsius zu erwärmen.
Wenn dann dieses 1 kg Wasser verdampfen soll, dann werden weitere 2.257,0 kJ an Wärmeenergie benötigt.
Hoppla, wenn 1 kg geschmolzenes Eis bis zum Siedepunkt erwärmt werden soll, sind 412 kJ erforderlich und zum Verdampfen mehr als das 5,4-fache!
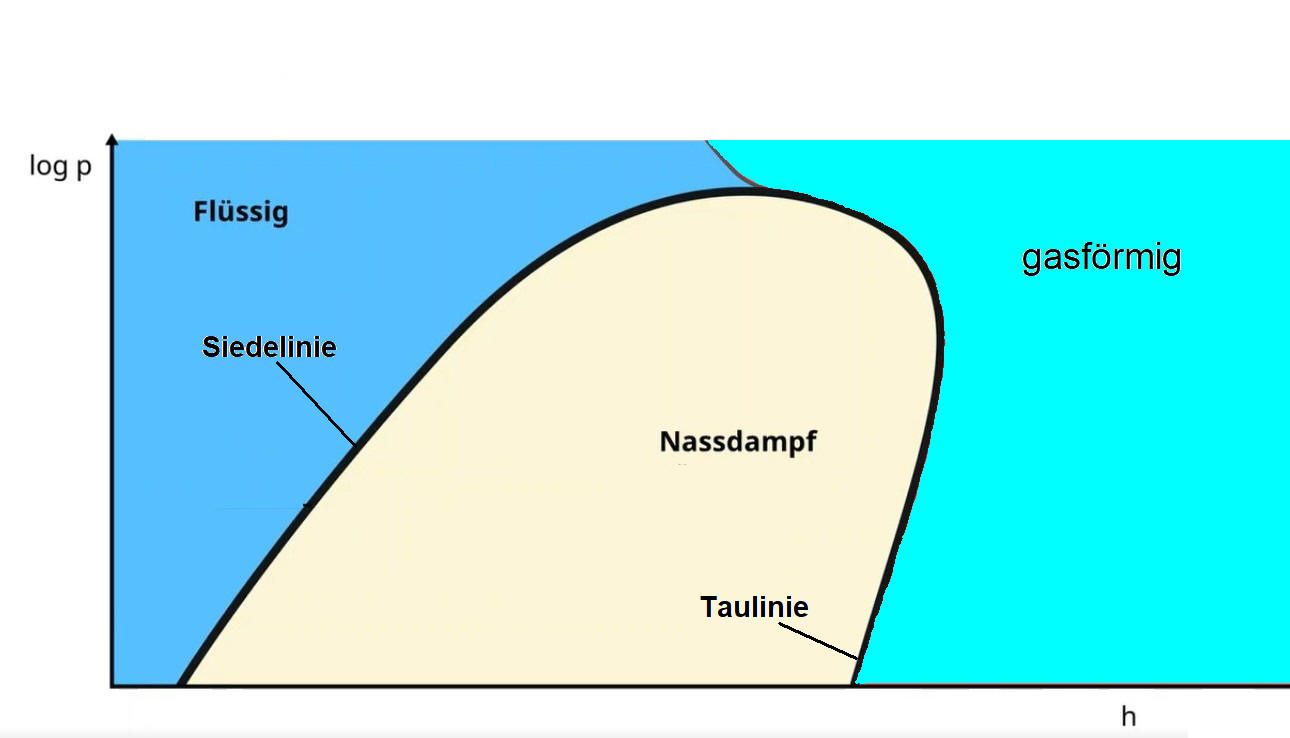
Weiter zum log p,h - Diagramm
Was ist das denn !?!
(log p) bedeutet lediglich, dass die senkrechte Achse mit dem Druck nicht linear abgebildet ist, d.h. der Abstand von 1 bar zu 2 bar ist größer als von 3 bar zu 4 bar - die Abstände von bar zu bar werden nach oben hin immer kleiner.
Die großen Vorteile bei diesem Diagramm sind zum einen der Überblick über große Druckbereiche und zum anderen können wir die Verdampfung bei verschiedenen Drücken betrachten.
Beim Vergleich dieses log p,h-Diagramms mit dem vorigen erkennen wir die Zustände flüssig, Nassdampf und gasförmig. Zudem sehen wir im unteren die Siede- und die Taulinie, die im oberen lediglich im Knick der Temperaturlinie als Punkt zu sehen sind.
Wenn wir diese Erkenntnisse von oben vereinigen, ...
... dann können wir folgendes überlegen:
Die Siedetemperatur lässt sich durch den vorhandenen Druck erhöhen, bzw. absenken. Jetzt trennen wir noch die beiden Bereiche voneinander, in denen die Flüssigkeit einmal verdampft und dann der Dampf wieder verflüssigt wird, und dann spendieren wir jedem Bereich einen eigenen Wärmetauscher. Damit können wir in jedem dieser beiden Bereiche die Arbeitsdrücke, einmal beim Verdampfen und beim Verflüssigen unabhängig voneinander einstellen.
Genau das war auch mal die Überlegung von Carl von Linde!
Er wollte in der Mitte des 19-ten Jahrhunderts auf diese Weise einen isolierten Raum herunterkühlen. Wir gehen jetzt noch einen kleinen Schritt weiter und bauen noch einen Umschalter in unsere Anlage ein, damit wir diesen "Sommerbetrieb" in einen "Winterbetrieb" umschalten können. Der isolierte Raum ist dabei unser Haus, das wir im Winter heizen und im Sommer vielleicht auch noch kühlen wollen.
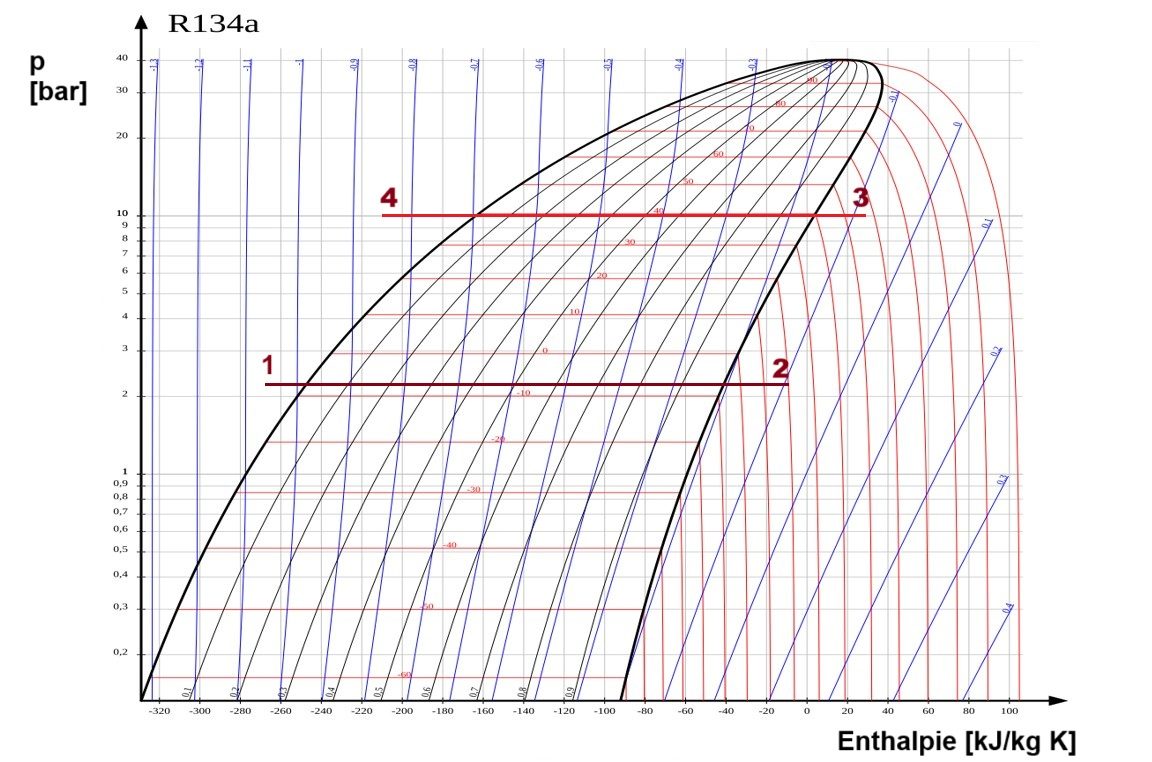
Der Kühlraum im log p,h - Diagramm
Unsere Temperaturen:
Die Kühlraum-Temp Tk = +2°C, die Außentemperatur Ta = +25°C.
Als Medium verwenden wir kein Wasser, sondern ein noch gängiges Kältemittel (R134a). Die Kühlschlangen des Verdampfers sollten ca. 10 K kühler sein als der Kühlraum, also -8°C und die Schlangen, die die Wärme draußen abgeben, planen wir ca. 15 K wärmer als die Außentemp., also +40°C.
Zu diesen Temp.-Werten holen wir uns aus der Dampfdrucktabelle von R134a die zugehörigen Drücke, die wir benötigen um unseren Siedepunkt bzw. den Taupunkt auf die gewünschte Temperatur zu bekommen.
Viele bunte Linien ....
.... und zwei, die uns interessieren!
Unsere beiden Linien sind mit Nummern markiert, jeweils Anfang und Ende.
Da wäre die untere Linie 1-2, sie liegt bei -8°C. Das ist die Linie, auf der wir unser Kältemittel verdampfen wollen, um dort der Luft des Kühlraumes die Wärme zu entziehen (Verdampfungswärme).
Zum anderen haben wir die obere Linie 3-4, die bei +40°C liegt und auf der wir unser Kältemittel wieder kondensieren, sprich verflüssigen wollen, um die Wärme wieder aus dem Kühlsystem zu bekommen. Die Höhe der Linien entspricht den Arbeitsdrücken im jeweiligen Wärmetauscher.
Der Druckunterschied liegt bei ca 8 bar. Um vom niedrigen auf das hohe Druckniveau zu kommen, brauchen wir einen Kompressor; also von Punkt 2 nach 3. Vom hohen zum niedrigen Druckniveau, 4 nach 1, benötigen wir eine sog. Drossel, die den Druck an ihrem Ausgang wieder absenkt.
Und siehe da: wir haben jetzt zwei Wärmetauscher, einen Kompressor und eine Drossel. Dies sind die Grundbestandteile eines Kühlaggregates, wie wir es in jedem Kühlschrank und jedem Gefrierschrank, bzw. in jeder Gefriertruhe, finden.
Ergänzen wir diese Maschine noch um ein 4-Wege-Ventil, damit wir die Wärmetauscher in ihrer Funktion, der Verdampfer und der Verflüssiger, vertauschen können, dann haben wir schon ein Klimagerät, das sowohl heizen als auch kühlen kann.
Das ist die grundlegende Funktionsweise von Wärmepumpen (Kühl- und Gefrierschränke, Klimageräte und auch Anlagen für Kühlräume).